Conceptos importantes

Enlaces ionicos: En estos enlaces los átomos pierden o ganan electrones para formar iones (cationes y aniones) y así obtener su configuración estable de 8 electrones en su último nivel. Cuando un átomo pierde electrónes se carga postivamente tantas veces como electrones pierda, por ejemplo el hierro Fe, puede perder 2 o 3 electrónes, por lo tanto puede formar iones que se simbolizan así: Fe2+ y Fe3+ , los iones positivos se forman con los metales y los iones negativos se forman con los no metales.
Veamos un ejemplo de ión negativo, el Flúor (F) puede ganar un electrón para obtener sus 8 electrónes de valencia, por lo tanto su ion se simboliza así: F-, esto indica que ha ganado 1 electrón. Observa la imágen en la que tenemos un átomo de sodio y un átomo de cloro que se cargan positiva o negativamente.

Representación de un enlace ionico
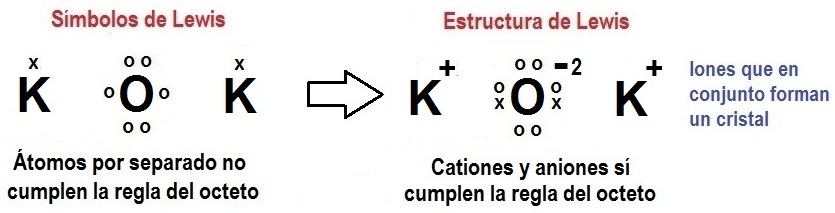
Imágen tomada de:http://4.bp.blogspot.com/-c2KIWy7jy1Y/TuaAPzWkReI/AAAAAAAAAeU/1U1yP-KZnx4/s1600/estructura%2Bde%2BLewis%2B9.jpg
Recurso tomado de:http://www.educaplus.org/play-77-Enlace-i%C3%B3nico.html









